- Index
- >Plateformes
- >LentiVec - Vecteurs lentiviraux
Plateforme de production de vecteurs lentiviraux

Présentation
Pôle
Biologie Santé - Service Commun
Présentation
La Plateforme LentiVec permet la construction à façon d’un vecteur lentiviral spécifique au gène d’intérêt que le chercheur souhaite exprimer. Plus généralement, elle fournit aux différentes équipes de recherche régionales et de la zone grand-ouest un savoir-faire et une expérience en transfert de gènes.
Parallèlement, LentiVec fait évoluer la technologie pour obtenir des vecteurs de meilleure efficacité et offrir de nouvelles applications aux clients.
Pour l’ensemble de ces techniques, LentiVec propose aux utilisateurs :
- Une aide à la définition des projets.
- La production en tout ou partie du vecteur lentiviral, selon la quantité demandée par le chercheur.
- La possibilité de réaliser soi même cette production au sein de la plateforme, selon les procédures établies.
- Une comptabilité analytique permettant la fourniture de devis et de factures à l’euro prêt pour chaque projet.
L’ensemble des prestations proposées et le fonctionnement de LentiVec s’inscrivent dans le cadre d’une démarche qualité, de respect des règles d’hygiène et de sécurité, et de garantie de la confidentialité des données.
Ces prestations respectent la législation en vigueur sur les organismes génétiquement modifiés.
Locaux
L’activité de production de vecteurs lentiviraux se fait au sein du bâtiment IBS-IRIS au CHU d’Angers. Elle est répartie dans 4 espaces séparés, ce qui permet un contrôle qualité de chaque étape de la production.
- Salle de bactériologie : 3ème étage, pièce 4118 : 12,63 m2
- Salle de biologie moléculaire : 2ème étage, pièce 3220 : 51,76 m2
- Laboratoire de confinement L2+ : 2ème étage, pièce 3242 : 41,76 m2
- Laboratoire de confinement L3 : 1e étage, pièce 2314 : 33 m2.

La plupart des manipulations se font dans un environnement classé L2. La production de lentivirus recombinants dont les inserts génomiques contiennent des oncogènes se fait dans un environnement L3. Ce laboratoire L3 est partagé avec le CHU, avec un accès dédié pour la plateforme LentiVec. Il est contrôlé régulièrement par l’APAVE.
Thèmes de recherche
Thèmes de recherche / expertise
-
Les vecteurs lentiviraux
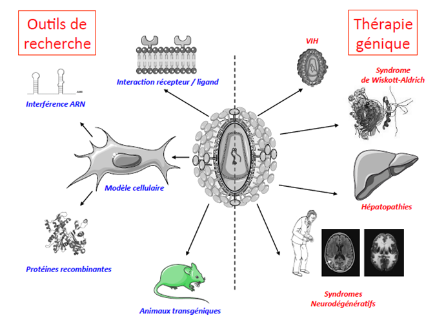
Les vecteurs lentiviraux (VL) sont des virus appartenant à un sous-groupe de la famille des rétrovirus dans lesquels la majorité des séquences virales codantes sauvages ont été délétées pour être remplacées par le gène d’intérêt, rendant ce vecteur défectif pour la réplication. Seules ont été conservées les séquences impliquées dans la transcription inverse, l’import nucléaire du génome viral et son intégration. Il s'agit du seul vecteur viral intégratif et non réplicatif disponible en pratique courante actuellement. Exprimé autrement, il s’agit du seul outil à notre disposition pour écrire dans le génome d’une cellule vivante, in vitro et in vivo.
Ainsi, outre le fait d’être un réel espoir en thérapie génique, le VL constitue également un puissant outil pour l’investigation et la compréhension de différents mécanismes en biologie. Ils ont en effet la particularité d’infecter efficacement un grand nombre de types cellulaires, permettant ainsi d'accéder à la compréhension des causes de la dérégulation des voies métaboliques par exemple, soit en sur-exprimant le gène candidat pour en étudier le gain de fonction au niveau cellulaire, soit en inhibant son expression à l'aide de molécules d'ARN interférentes ou l'expression d'antagonistes (dominants-négatifs), ou encore en invalidant directement le gène à l’aide de nucléases artificielles (approche d’édition de gènes). Leurs propriétés d'expression d'un gène modulable à la fois qualitativement et quantitativement peuvent aussi être employés pour produire en grande quantité des protéines thérapeutiques, notamment celles qui présentent des modifications post-traductionnelles complexes pour être actives.
En raison de leurs propriétés, les VLs offrent également des perspectives très prometteuses in vivo. Identifier les cellules souches à l’origine de l’architecture tissulaire et fonctionnelle d’un organe différencié et quiescent peut permettre d’envisager leur expansion in vitro pour leur réimplantation dans cet organe dans le cas d’une dégénérescence cellulaire (dégénérescence maculaire, syndrome d’Alzheimer …). Inversement, la connaissance de l’origine de cellules qui prolifèrent de façon anarchique peut laisser espérer une action préventive efficace et ciblée en ayant identifié au préalable des moyens de les discriminer parmi les cellules saines. La méthode de lignage cellulaire consistant à identifier l’origine des cellules est facilitée par les techniques de marquage génétique in vivo à l’aide des VLs, grâce à des gènes marqueurs codant une protéine facilement détectable par immunohistochimie. Dans une thématique sensiblement proche, il est possible de différencier efficacement des cellules souches pluripotentes en un type cellulaire souhaité ou de reprogrammer des cellules adultes en cellules souches pluripotentes. Dans les deux cas, les gènes responsables de la transition phénotypique d'un type cellulaire à l'autre, principalement des facteurs de transcription, peuvent être exprimés à l'aide de VLs.
Savoir-faire
Prestations de services
- Production
La production de vecteurs lentiviraux se décompose en 4 grandes étapes : ·
- la production d'ADN plasmidique correspondant aux plasmides vecteur, d'encapsidation et d'enveloppe
- l'amplification des cellules d’encapsidation et leur transfection,
- la récolte des particules virales et leur purification suivie d'une concentration
- leur titration.

Cette production fait appel à trois disciplines :
- la bactériologie (amplification de plasmides)
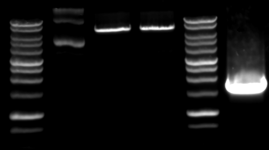
- la biologie moléculaire (construction génomique)
- la biologie cellulaire.

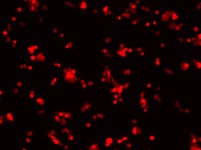
Grâce à une collaboration étroite avec la PACeM, les techniques de cytométrie en flux ont permis la mise au point d’un système de titration en flux rapide et fiable permettant la titration en routine et en série de grande quantité de vecteurs lentiviraux. Ce système de tri cellulaire est en mesure de dissocier des cellules infectées par des VL qui expriment un gène rapporteur fluorescent en fonction de l’intensité de cette de fluorescence. Parallèlement, toujours avec la PACeM, une quantification par qPCR a été développée et en cours d’amélioration.
Contacts
Adresse postale
LentiVec Bâtiment IBS-IRIS (2ème étage) CHU Angers 4, rue Larrey 49933 Angers Cedex 09
Contacts